Linfoma Primario del SNC
RESUMEN
Los linfomas primarios del SNC (LCP) son tumores cerebrales infrecuentes y de comportamiento agresivo. Son linfomas no Hodgkin extraganglionares que se desarrollan primariamente en el cerebro, la medula espinal, los ojos y las leptomeninges. Pueden aparecer tanto en pacientes inmunodeprimidos como inmunocompetentes.
Sus manifestaciones típicas son las de cualquier lesión ocupante de espacio del SNC de evolución subaguda, aunque las crisis comiciales son menos frecuentes que en otros tumores cerebrales. La RM suele mostrar una masa única o múltiple, localizada preferentemente en los hemisferios cerebrales, con captación homogénea de contraste y restricción de la difusión, pudiendo aparecer en pacientes inmunodeprimidos imágenes de necrosis central y captación en anillo tras la administración de contraste. La biopsia cerebral es fundamental para confirmar el diagnóstico. Una vez confirmado, debe realizarse estadificación de la enfermedad para establecer su extensión y confirmar que sólo afecta al SNC. Para ello se recomienda la exploración física (búsqueda de adenopatías y/u organomegalias); analítica de rutina; serología VIH; punción lumbar con citología y citometría de flujo; examen oftalmoscópico con lámpara de hendidura; body-TAC; biopsia de médula ósea y ecografía testicular (en pacientes mayores).
Las opciones de tratamiento disponibles son los corticoides, la quimioterapia y la radioterapia. La resección tumoral no tiene indicación, salvo si existe riego de herniación por el efecto de masa. La pauta de tratamiento más habitual consiste en la administración de quimioterapia (intravenosa e intratecal o intraventricular) seguida de RT holocraneal (40-45 Gy). La mayoría de las pautas de quimioterapia incluyen como agente básico el metotrexate (a dosis de 2-3 g/m2) asociado a agentes como citarabina, vincristina, procarbazina, BCNU, etopósido y corticoides. Aunque la toxicidad del tratamiento no es despreciable, la tasa global de respuesta es del 80-90%, la mediana de tiempo hasta la progresión es de 2-3 años y la supervivencia media se acerca a los 4 años. La afectación tardía de la sustancia blanca (leucoencefalopatía) es variable, presentando mayor riesgo los mayores de 60 años.
Los factores pronostico más importantes en el LCP son la edad y el estado general del paciente.
DEFINICIÓN Y EPIDEMIOLOGÍA
Los linfomas primarios del Sistema Nervioso Central (LCP) son aquellos linfomas no Hodgkin (LNH) extraganglionares que se desarrollan en el cerebro, la médula espinal, los ojos y las leptomeninges, y en los que no existe evidencia de afectación sistémica ni antecedentes de linfoma sistémico. Son un grupo de tumores muy graves y agresivos, mortales, sin tratamiento curativo y con una mediana de supervivencia bajo tratamiento sintomático de 1,9-3,3 meses (Gómez Codina; 2008).
Los LCP son una enfermedad rara con una incidencia estimada de 0.46-0.47 por 100.000 habitantes y año. Suponen en torno al 3% de todos los tumores primarios del SNC. En las décadas de 1970-1980 su incidencia aumentó con la aparición de la infección por VIH, con un incremento importante entre los pacientes gravemente inmunodeprimidos. Con la mejora del tratamiento antirretroviral esta incidencia ha disminuido. Los LCP también se han asociado a inmunosupresión terapéutica en pacientes trasplantados (1-5%) y en inmunodeficiencias genéticas (síndrome de Wiskott-Aldrich). Por último, parece haberse producido también un incremento entre la población inmunocompetente, en especial los mayores de 60 años, sin que exista una explicación clara (Vilar et al; 2008).
FACTORES PRONÓSTICO
Los únicos factores cuya importancia pronóstica se repiten en todos los estudios son la edad y el estado general del paciente.
Se han desarrollado varios índices pronóstico específicos para los pacientes con LCP, como el del Memorial Sloan-Kettering Cancer Center cuya utilidad se ha validado (Abrey et al, 2006). Este índice divide a los pacientes en tres grupos en función de la edad y su estado general: aquéllos menores de 50 años; mayores de 50 y un Karnofsky Performance Score (KPS) >70; mayores de 50 y KPS <70. Basándose en estas divisiones hay diferencias significativas en supervivencia global y libre de enfermedad, siendo el pronóstico más favorable para los más jóvenes y en mejor estado.
MANIFESTACIONES CLÍNICAS
Los síntomas corresponden a los de una lesión expansiva intracraneal de evolución subaguda (síntomas neurocognitivos y alteraciones comportamentales, hipertensión intracraneal, focalidad motora, crisis…). Las crisis son menos frecuentes que en otros tipos de tumor cerebral y aparecen en un 14% de los casos. Al contrario que en los linfomas sistémicos, no suelen aparecer síntomas B.
El linfoma ocular se manifiesta con borrosidad visual o “cuerpos flotantes” y se puede manifestar antes, durante o después del diagnóstico de LCP.
EVALUACIÓN DIAGNÓSTICA
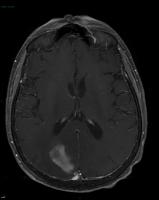
En el diagnóstico por RM suele observarse una masa única o múltiple, localizada preferentemente en los hemisferios cerebrales, con captación homogénea de contraste [Imagen RM con contraste de LCP.jpg]
y restricción de la difusión [Imagen RM difusión de LCP.jpg].
En pacientes inmunodeprimidos pueden observarse lesiones con necrosis central y captación en anillo tras la administración de contraste.
La prueba diagnóstica imprescindible es la biopsia cerebral, que no sólo permite establecer el diagnóstico, sino también determinar el subtipo histológico del linfoma. La técnica de elección es la biopsia esterotáxica.
Una vez establecido el diagnóstico definitivo de LCP debe realizarse una estadificación. Su objetivo es establecer la extensión de la enfermedad en el momento del diagnóstico y confirmar que tan sólo afecta al SNC. Para ello se recomienda exploración física con búsqueda de adenopatías y/u organomegalias; analítica de rutina; serología VIH; punción lumbar con citología y citometría de flujo (ya que hay afectación leptomeníngea en el 15-30% de los casos); examen oftalmoscópico con lámpara de hendidura; body-TAC; biopsia de médula ósea y ecografía testicular (en pacientes mayores).
TRATAMIENTO INICIAL
Las opciones de tratamiento disponibles son los corticoides, la quimioterapia y la radioterapia. La cirugía resectiva no tiene indicación, salvo en aquella circunstancia donde haya riego de herniación por el efecto de masa.
- Corticoides
Aunque su efecto es rápido pudiendo ocasionar regresión tumoral y descenso del edema peritumoral, estos fármacos deben ser retirados o no iniciarse antes de la biopsia porque pueden dificultar el diagnóstico histológico (Gestner et al; 2010).
A pesar de la respuesta inicial, la mayoría de los pacientes recaen y requieren otras alternativas de tratamiento. No obstante, una respuesta radiológica tras los corticoides se ha planteado como un marcador pronóstico favorable.
- Radioterapia (RT)
La radioterapia holocraneal fue tradicionalmente la forma de tratamiento de este tumor; sin embargo, administrada en solitario es inadecuada, sobre todo para pacientes con afectación leptomeníngea. Se observa una respuesta radiológica inicial en un 90% de pacientes, pero la recaída aparece en unos meses. La supervivencia media de pacientes tratados con RT sin quimioterapia es de 12-18 meses y la supervivencia a cinco años varía del 18-35% (Gestner et al; 2010).
- Quimioterapia (QT)
Dados los escasos resultados del tratamiento clásico basado en corticoides y RT se empezaron los primeros trabajos con quimioterapia.
- Quimioterapia sistémica
Inicialmente se ensayaron los esquemas de QT similares a los empleados en LNH sistémicos y, posteriormente, se desarrollaron los esquemas de metrotrexate (MTX) a dosis altas. Administrado como agente único a dosis >1 g/m2 por vía endovenosa se consiguen tasas de respuesta del 30-80%, aunque las recidivas son frecuentes (Gerstner et al., 2008; Hoang-Xuan et al.; 2003). Se están introduciendo otros fármacos junto con el metrotrexate como la vincristina, procarbazina, rituximab, tiotepa, nitrosoureas, tenopósido y, sobre todo, arabinósido de citosina (Vilar et al; 2008).
- Quimioterapia intratecal
Teniendo en cuenta que la afectación meníngea es relativamente frecuente en el curso de los LCP, la QT intratecal se consideraba parte importante del tratamiento. Hoy en día esta cuestión está en entredicho y no parece ser estrictamente necesaria cuando se emplean dosis de MTX superiores a 3 g/m2. No obstante, para los pacientes con afectación leptomeníngea documentada el tratamiento intratecal se recomienda y la administración vía Ommaya® es la forma más segura y eficiente de administrarla (Gestner et al; 2010).
- Terapia combinada
La mayoría de los grupos optan por administrar QT (intravenosa e intratecal o intraventricular) seguida de RT. La mayoría de las pautas incluyen como agente básico el MTX (a dosis de 2-3 g/m2) asociado a agentes como citarabina, vincristina, procarbazina, BCNU, etopósido y corticoides; seguido de RT holocraneal (40-45 Gy). Aunque la toxicidad no es despreciable (5-10% de muertes durante el tratamiento y 3-12% de toxicidad neurológica diferida), la tasa global de respuesta es del 80-90%, la mediana de tiempo hasta la progresión es de 2-3 años y la supervivencia media se acerca a los 4 años (Vilar et al; 2008).
Esta modalidad de terapia combinada es mucho más tóxica en mayores de 60 años, lo que ha llevado a cuestionar la idoneidad de la RT en este grupo de pacientes.
TRATAMIENTO DE LAS RECAÍDAS
La mayor parte de los pacientes recaen y para ellos no hay un tratamiento estándar. En aquellos que no recibieron RT en la primera línea, ésta puede ser una buena opción. Cuando el tratamiento inicial con MTX produjo una buena respuesta y la recaída es tardía, puede ensayarse el retratamiento con MTX a dosis altas. También se han ensayado fármacos de segunda línea (p.ej. arabinósido de citosina, vincristina y fármacos nuevos) (Gómez Codina; 2008).
NUEVOS TRATAMIENTOS
Entre estos tratamientos nuevos cabe destacar la QT intensiva con soporte de progenitores hematopoyéticos autólogos que se ha ensayado como consolidación en la primera línea tras la inducción con MTX, o como parte del rescate en las recaídas.
Otra opción es aumentar la permeabilidad de la barrera heamatoencefálica mediante la infusión intraarterial de manitol seguida de una combinación de fármacos (ciclofosfamida, altas dosis de MTX, procarbazina y dexametasona).
NEUROTOXICIDAD
La afectación tardía de la sustancia blanca (leucoencefalopatía) es variable (5-36%) y el mayor riesgo lo tienen los mayores de 60 años.
Clínicamente consiste en un deterioro cognitivo progresivo, psicosis orgánica, ataxia y alteraciones esfinterianas hasta una demencia totalmente incapacitante.
Parece ser que es el tratamiento combinado el responsable de esta grave complicación y se han propuesto estrategias diversas como reducir la dosis total de irradiación hasta 23,4 Gy, pero sin resultados hasta la fecha (Gómez Codina; 2008). No hay tratamiento eficaz para el trastorno y puede incluso llegar a ser mortal.
BIBLIOGRAFÍA
Vilar S, Gil Gil M (2008). En: Publicaciones Permanyer. Linfoma cerebral primario. Protocolo de los Tumores del Sistema Nervioso (97-101).
Gómez Codina J. (2008). Linfomas cerebrales. En: Publicaciones Permanyer 2008. Tumores cerebrales. Manual Práctico 2008 (337-359).
- 38897 lecturas